ПЭТ КТ с аминокислотными радиомаркерами метионином, тирозином и их аналогом ФДОПА является ведущим методом диагностики в нейроонкологии. Позволяет определить точную локализацию первичных интракраниальных опухолей, их распространенность и стадии злокачественного процесса.
Неоспоримое достоинство исследования – возможность дифференцировать опухолевые и неопухолевые процессы, разграничивать рецидивы рака и индуцированные терапией изменения в тканях (инфаркты мозга, псевдопрогессию, псевдоответ, радиационный некроз), что особенно важно для оценки эффективности проводимого лечения.
Цены на ПЭТ КТ нейроонкологического профиля
| Наименование лечебного учреждения / Телефон | Область исследования / радиофармпрепарат (РФП) | Цена |
|---|---|---|
Центр ядерной медицины «ПЭТ-Технолоджи» в Балашихе Московская область, Балашиха, ул. Карбышева, д. 6Б | ПЭТ/КТ головного мозга с тирозином (18F-FET) | 62 000 руб. |
Воронеж, ул. Остужева, 31 | ПЭТ/КТ головного мозга с тирозином (18F-FET) | 49 000 руб. |
Центр ядерной медицины «ПЭТ-Технолоджи» в Уфе Уфа, ул. Рихарда Зорге, д. 58, к. 2 | ПЭТ/КТ головного мозга с тирозином (18F-FET) | 84 200 руб. |
Стоимость обследования по аналогичному протоколу может различаться и зависит от позиционирования центра, дополнительных услуг, акционных предложений, а также компетентности радиологов.
Позвоните по указанным телефонам или свяжитесь с нами через форму на этой странице, и наши координаторы ответят на интересующие вас вопросы, проинформируют о необходимом пакете документов, помогут организовать бесплатную консультацию врача-эксперта, запишут на обследование без очереди.
Где еще можно сделать исследование

Сканирование с метионином ( 11C-MET) также проводится в:
- Национальном медицинском исследовательском центре нейрохирургии имени академика Н.Н.Бурденко;
- Национальном медицинском исследовательском центре сердечно-сосудистой хирургии имени А. Н. Бакулева;
- ФГБУ «Национальный медицинский исследовательский центр им. В.А. Алмазова;
- ФГУ «Российский научный центр радиологии и хирургических технологий имени академика А.Н. Гранова;
- Институте мозга человека;
- Европейском Медицинском Центре.
Сканирование с тирозином (18F-FET) выполняют в:
- ФГБУ «Российский онкологический научный центр им. Н. Н. Блохина»;
- Европейском Медицинском Центре
Исследование с ФДОПА (18F-FDOPA) проводится в:
- ФГБУ «Национальный медицинский исследовательский центр им. В.А. Алмазова;
- Европейском Медицинском Центре.
В таблице представлены цены на ПЭТ КТ исследование головного мозга в российских центрах ядерной медицины.
Базовая стоимость услуг зависит от используемого радиофармпрепарата, протокола исследования, технических характеристик оборудования.
Показания для проведения ПЭТ КТ с метионином и другими аминокислотными радиоизотопами
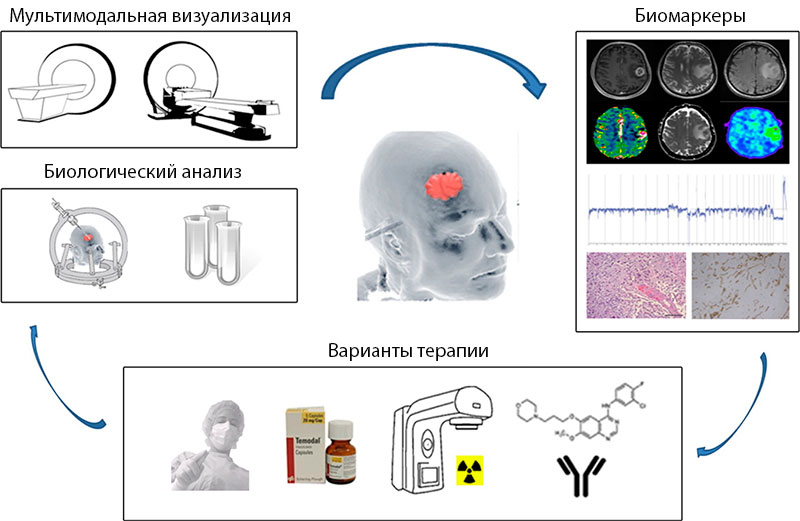
Направления применения ПЭТ КТ при злокачественных образованиях головного мозга
ПЭТ КТ с метионином (11C-MET) обеспечивает биохимические и физиологические данные о неопластических образованиях мозга с четкой их локализацией.
Это позволяет использовать методику при первичных интракраниальных опухолях не только для точного определения местоположения, распространенности и градации опухоли, но и для оценки эффективности оперативного лечения, радио- и химиотерапии.
Неоспоримым достоинством исследования является возможность дифференцировать опухолевые и неопухолевые процессы, а значит – отличать рецидивы рака и индуцированные терапией изменения в тканях (псевдопрогессию, радиационный некроз и т.д.).
Единственный недостаток этого фармпрепарата – короткий период полураспада 11С изотопа углерода (20 мин), что ограничивает его применение только центрами с циклотронами и лабораториями радиосинтеза.
Это способствовало разработке 18F-меченных трассеров, период которых достигает 110 минут. Среди них самых наиболее распространены 18F-фторэтил-L-тирозин (FET) и аминокислотный аналог 3,4-дигидрокси-6-(18) F-фтор-L-фенилаланин (FDOPA).
Показания для ПЭТ КТ с изотопами 18F не отличаются от таковых для метионина. Они также используются для определения распространенности опухоли, выявления рецидивов рака с целью прогнозирования заболевания для подбора риск-адаптированной терапии и ее контроля.
При проведении исследования с тирозином возможна динамическая оценка накопления этого радиоизотопа, что используют для определения стадий рака с большей точностью. Для низкозлокачественных глиом (grade II) характерны постепенная динамика захвата ФЭТ с нарастающими кривыми время-активность, в отличие от раннего максимального периода активности для опухолей III/IV стадий.
Пример:
По результатам динамического сканирования ПЭТ КТ с 18F-FET были построены кривые время-активность для стадирования типичной астроцитомы (grade II, синяя кривая), анапластической астроцитомы (grade III, красная кривая) и глиобластомы (grade IV, зеленая кривая)
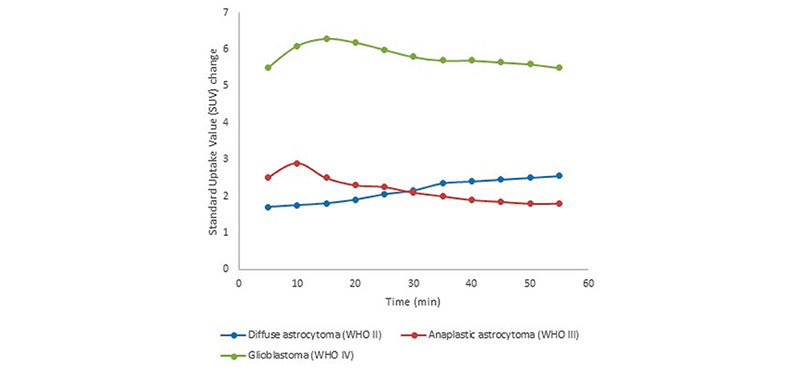
Стадирование по результатам динамической ПЭТ-КТ
Методика используется также при миеломной болезни, лимфомах и лимфогранулематозе.
Появились данные о возможности применения методики для направленной радиолигандной терапии рака мозга и выявления деструктивных очагов при резистентной эпилепсии.
В таблице представлены показания к исследованию на различных этапах диагностики и терапии, а также в периоде наблюдения.
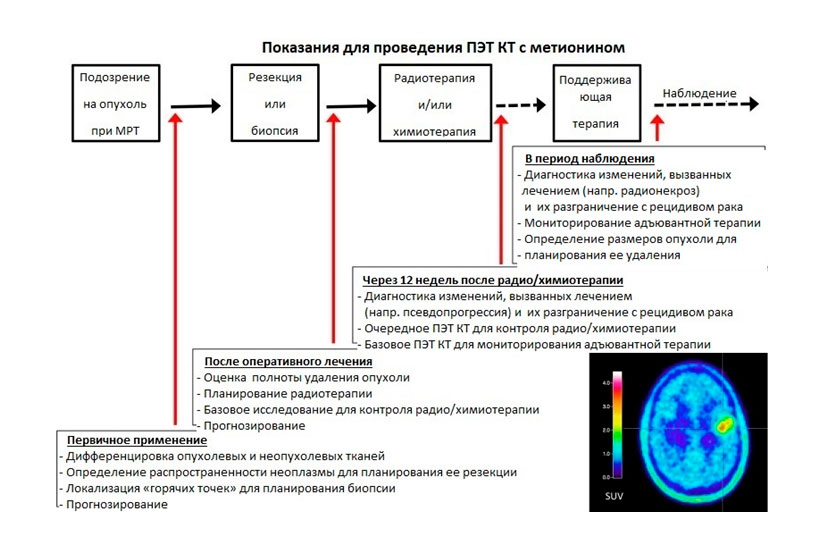
Как проходит процедура
Во время первичного приема радиохирург ориентируется на следующие данные:
- Четко обоснованные показания для ПЭТ КТ головного мозга;
- Клиническую информацию о пациенте, в том числе о приеме лекарственных средств, включая глюкокортикоиды, для правильной интерпретации исследования и во избежание нежелательных эффектов фармакологического взаимодействия, если необходима легкая седация;
- Историю предшествующей терапии, включая хирургическое вмешательство, лучевую и химиотерапию, которые могут повлиять на распределение радиофармацевтических препаратов;
- Результаты визуализирующих исследований, выполненных резекций и биопсий, а также лабораторных тестов;
- Скрининг по наличию противопоказаний с использованием стандартизированной анкеты: беременность, кормление грудью, реакции на контрастные вещества, клаустрофобия и т.д.
Подготовка пациента и меры предосторожности
- Рост и масса тела пациента документируются для расчета радиофармацевтического препарата и измерения стандартизированных значений поглощения (SUV);
- Пациента информируют о процедуре, для осознанного соблюдения правил с целью минимизации погрешностей и оптимизации результатов сканирования;
- Пациент должен быть в состоянии спокойно лежать в течение не менее 30-40 минут;
- Если для получения изображений MET, FET или FDOPA требуется седация, ее начинают примерно за 20–60 минут до обследования;
- Пациент прекращает прием пищи за 4-6 часов до начала обследования для стабилизации метаболических условий;
- Желательно накануне соблюдать безбелковую диету, употребляя в пищу овощи, фрукты и отказавшись от молока, мяса, рыбы, бобовых;
- Рекомендуется хорошая гидрация пациента с предпочтительным приемом чистой воды и частое опорожнение мочевого пузыря до обследования;
- Перед сканированием пациентам следует опорожнить мочевой пузырь для максимального комфорта во время исследования и для уменьшения поглощенной дозы в мочевом пузыре;
- Для исследования с FDOPA премедикация карбидопой не требуется. Большинство опубликованных исследований FDOPA ПЭТ у пациентов с опухолью головного мозга не использовали карбидопу или другие ингибиторы периферического метаболизма FDOPA;
- Рекомендуется комфортная, теплая одежда.
Положение пациента
Пациент располагается на спине, руки вытянуты вдоль тела. Голова стабилизирована в удобном положении на подголовнике, возможно использование других гибких держателей. Весь мозг, включая мозжечок, должен быть в поле зрения, для чего следует избегать чрезмерного разгибания или сгибания шеи.
Во время исследования пациент должен быть расслаблен, спокоен и постоянно находиться под визуальным наблюдением. Мониторинг особенно важен у пациентов с судорогами, связанными с опухолью. Судорожная активность во время фазы поглощения радиомаркеров может привести к увеличению захвата радиотрассера в зоне мозга с повышенной активностью и привести к ложноположительному результату.
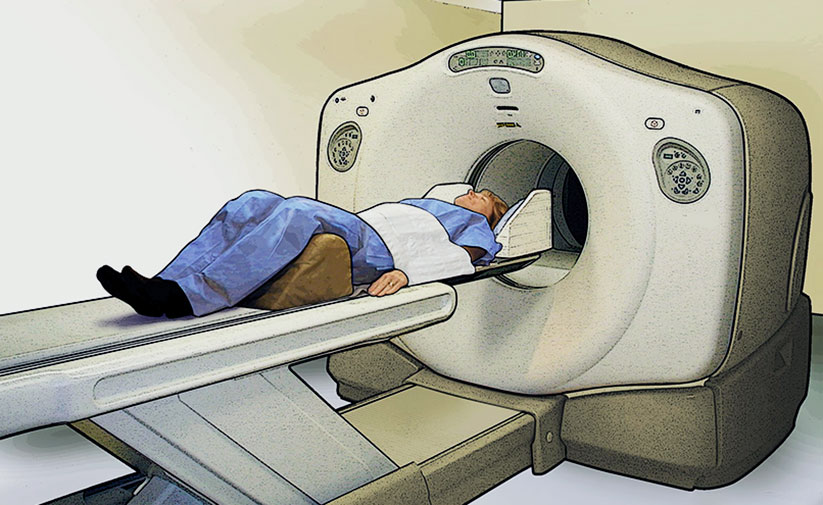
Положение пациента для ПЭТ КТ головного мозга
Протокол исследования
Препарат вводится внутривенно болюсно с последующей промывкой вены небольшим количеством физиологического раствора.
Рекомендуемая дозовая активность фармпрепарата у взрослых
| 18F-FET: 185–200 МБк; | 11C-MET: 370–555 МБк; | 18F-FDOPA: 185–200 МБк |
Спустя некоторое время начинается сканирование по стандартным протоколам в зависимости от вводимого радиофармпрепарата:
- 18F-FET — 20 минут статического изображения через 20 минут после инъекции. Оно может быть также частью динамического изображения в течение 40–50 минут после введения индикатора;
- 11C-MET — 20 минут статического изображения через 10 минут после инъекции;
- 18F-FDOPA — 10–20 минут статического изображения через 10–30 минут после инъекции.
Истории пациентов
Пациентка 52 лет с глиальной опухольюЖенщина 52 лет, которая больше года наблюдалась у нейрохирургов с подозрением на опухоль головного мозга. Проведенные магнитно-резонансные исследования не позволяли однозначно трактовать картину заболевания. После появления возможности более точного обследования, пациентке было назначено ПЭТ КТ с 18F-FET. Сканирование четко выявило очаг в правой лобной доле, который оказался высокодифференцированной глиальной опухолью с низкой степенью злокачественности. Это позволило своевременно провести лечение с высокой степенью положительного прогноза.
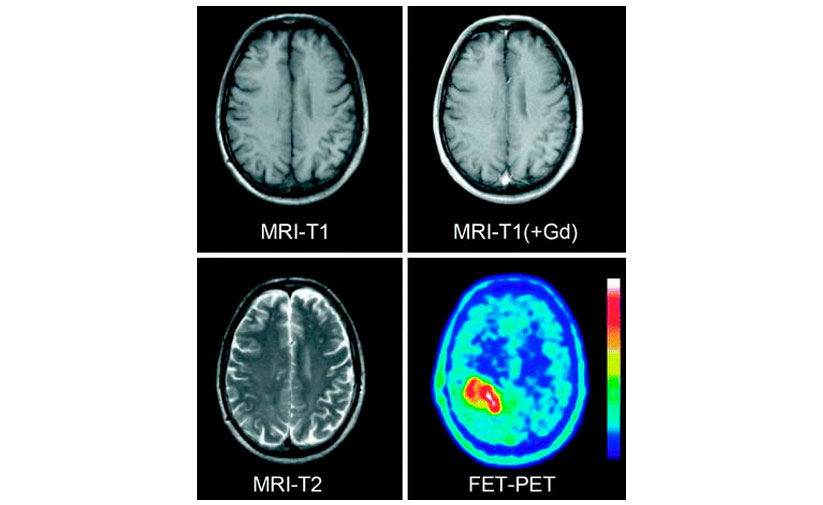
Преимущества визуализации опухоли мозга при ПЭТ КТ с тирозином по сравнению с МРТ
пациент Райан, 16 лет, очаговая кортикальная дисплазияВ возрасте 3 лет родители Райана были обеспокоены, когда его правая нога начала подрагивать в течение одного-двух дней, мальчик в шутку ее называл: «моя волнистая нога». А к 10 годам, когда приступы уже охватывали всю правую половину тела, ему был выставлен диагноз идиопатической эпилепсии. Райану была назначена противосудорожная терапия, которая уменьшила частоту и силу приступов, но не устранила их. Со временем ситуация начала ухудшаться, но коктейли лекарственных средств не давали эффекта и в 16 лет после жестокого приступа была парализована вся правая сторона. Лекарственная резистентность оставляла только один путь решения проблемы – хирургический, однако множественные МРТ исследования не выявляли структурного поражения мозга. Нейрохирург решил продолжить поиск и назначил ПЭТ КТ с метионином. И только тогда был обнаружена маленькая зона повреждения: — «Это было похоже на слезинку клеток на дне извилины в лобной доле коры головного мозга, очень близко к левой моторной полоске, которая контролирует движение правой стороны тела». Хотя риски оперативного лечения были высоки, ведь очаг располагался очень в нескольких миллиметрах от зон мозга, ответственных за речь и движения, но профессионализм врачей и современная система нейронавигации позволили эффективно устранить причину болезни.
Противопоказания, побочные эффекты
Метод практически не имеет абсолютных противопоказаний, за исключением беременности и кормления грудью.
Обследование может быть затруднено при неспособности пациента контролировать положение тела, поскольку это вызывает значительные погрешности изображения.
Рекомендуемый минимальный интервал после предыдущего лечения (химиотерапия, хирургическое лечение) – не менее 10 дней, а после лучевой терапии – не менее 2-3 месяцев. Это необходимо для уменьшения артефактов, связанных с аномальным накоплением радиофармпрепарата в зонах индуцированного воспаления.
Радиационное облучение
Назначение процедуры всегда требует оценки соотношения риска и диагностической ценности, и оправданно лишь при их адекватности.
Несмотря на то, что эта процедура объединяет два исследования, получаемая доза облучения при стандартном протоколе даже несколько меньше, чем при диагностической компьютерной томографии.
Применяемые радиофармпрепараты имеют очень небольшое время полураспада – 20 минут для 11C-MET и 110 минут для 18F-FET, 18F-FDOPA, то есть через 20-110 минут уровень радиации снижается наполовину. Это приводит к быстрому снижению уровня радиации сразу после окончания исследования. А поскольку основное количество вещества аккумулируется в целевых органах, то воздействие биомаркера на весь организм незначительно. Риск для органов накопления расценивается как низкий или умеренный, в зависимости от протокола и количества контрольных исследований. Продукты метаболизма радиотрассеров естественны для организма и не имеют на него отрицательного влияния.
Побочные эффекты
Как правило, ни аллергических, ни токсических эффектов при этой процедуре не наблюдается.
Позвоните нашему координатору для записи на диагностику и определения перечня необходимых документов и предварительных исследований.
Решение об обоснованности назначения будет принято на основании доступных данных предыдущих исследований, анамнеза заболевания.
При необходимости дополнительных тестов, вам четко их перечислят и помогут провести и в сжатые сроки в лучших специализированных учреждениях.
Описание особенностей методики
Базовым методом выявления и контроля терапевтической эффективности при лечении неопластических образований головного мозга является магнитно-резонансная терапия, поскольку она дает точную информацию о нормальной и патологической анатомии головного мозга. Тем не менее, МРТ имеет заметные ограничения в определении инфильтрации опухоли в окружающие ткани и в посттерапевтическом мониторинге. Существует достаточно большая группа опухолей, визуализация которых затруднена даже при МРТ с контрастированием.
Поэтому, во многих случаях, лишь молекулярно-функциональное исследование может визуализировать биологические процессы пролиферации, мембранного биосинтеза, потребления глюкозы и аминокислот, характерные для злокачественно переродившихся клеток.
Для устранения диагностических ограничений МРТ были синтезированы многочисленные радиофармацевтические препараты, которые используются для совмещенной позитронно-эмиссионной/ компютерной томографии при опухолях головного мозга.
Широко распространенное исследование ПЭТ КТ с фтордезоксиглюкозой (ФДГ) при интракраниальной локализации рака не дает гарантии точной диагностики, поскольку глиомы (grade II и III) и дизембриопластические нейроэпителиальные опухоли (grade I) в большинстве своем ФДГ-негативны
Поглощение 18F-FDG увеличивается не только при опухолевом росте, но также характерно для инфекционных и воспалительных процессов. То есть, эта методика неспецифически отражает высокий метаболизм глюкозы, а не неопластические процессы.
Да и высокая активность поглощения глюкозы нормальными клетками мозга ограничивает применение этого радиомаркера.
Поэтому возникла необходимость в биомаркерах с большей специфичностью для злокачественного роста.
Основное преимущество аминокислотных ПЭТ-трассеров заключается в значительно большем поглощении их тканями опухолей по сравнению с низким потреблением здоровыми тканями мозга. В результате существенно увеличивается контрастность канцерогенных очагов по отношению к фоновой контрастности
11C-MET (радиоизотоп естественной для нашего организма аминокислоты – метионина) – один из наиболее эффективных трассеров для этих целей.
Синтез протеинов является краеугольным камнем роста и размножения. Метионин – это важнейшая аминокислота, необходимая не только для образования белков, но и для фосфолипидного синтеза.
С помощью радиоизотопа 11С можно неинвазивно проследить потребление метионина при ПЭТ исследовании. Доказано высокое поглощение метионина целым рядом опухолей, что связано с системой крупных транспортеров аминокислот LAT-1.
Ниже представлены специфические рекомендации для применения 11C-MET и других аминокислотных радиотрассеров.
Первичная диагностика/дифференциальный диагноз
Основное применение 11C-MET – это выявление неоплазм центральной нервной системы и лимфом с высокой чувствительностью (97%) без ложноположительных находок.
Гораздо более высокая степень накопления метионина глиальными и эпителиальными опухолями по сравнению с окружающими тканями используется в неинвазивной дифференцировке опухолевых и неопухолевых процессов.
Хотя умеренное накопление метионина характерно для доброкачественных заболеваний мозга (напр. острых воспалительных процессов, кавернозных мальформаций, инфарктов мозга и т.д.), но стандартизованный уровень накопления (SUV) и отношение контрастности поражения к фоновой нормальной ткани в подавляющем большинстве случаев значительно выше при злокачественных процессах, что позволяет провести разграничение патологии.
Определение стадии злокачественного процесса
ПЭТ КТ с метионином предоставляет информацию, необходимую для определения степени злокачественности рака, поскольку его накопление неоплазмами увеличивается с прогрессированием заболевания.
Безусловно, уровень захвата маркера не всегда стабилен, бывают ситуации, когда он сходен при различных стадиях канцера, что может зависеть от его гистологических подтипов.
Точность определения стадий рака может быть улучшена при оценке динамики накопления. Для низкого класса процесса (grade II) характерны постепенно нарастающие кривые время-активность, в отличие от раннего периода активности для опухолей III/IV классов.
Оценка распространенности
Благодаря тому, что эта методика дает функциональную и метаболическую информацию об опухоли, возможна идентификация зон инфильтрации канцером с четким разделением опухоли, отека и нормальной ткани мозга.
Так, при II стадии, большинство неоплазм имеют инфильтративные края, которые не определяются при магнитно-резонансной терапии, и только ПЭТ КТ с аминокислотными радиомаркерами позволяет четко очертить границы патологического роста.
Этот метод исследования имеет преимущества и при III/IV стадиях рака, поскольку более надежен в оценке объема опухолей: в среднем, зона распространения определяется на 2-3,5 см больше, чем при МРТ с контрастным усилением.
Планирование лечения: биопсия и резекция
Совмещенное позитронно-эмиссионное и компьютерное сканирование имеют неоспоримые преимущества для планирования биопсии и удаления опухолей, поскольку четко определяют их размер и границы.
Более того, при этом выявляется внутриопухолевая неоднородность с выделяющимися «горячими точками» злокачественных очагов. А значит, при направленной биопсии производится забор тканей из максимально биологически агрессивной зоны, что существенно влияет на прогноз и лечебную тактику.
Возможность точного определения границ патологического процесса, выявления вовлеченности функционально значимых областей мозга и высокозлокачественных зон, имеют определяющее значение для планирования объема оперативного вмешательства и снижают риск неполного удаления канцера.
Планирование лечения: радиотерапия
По границам поглощения радиофармпрепарат определяется биологический объем опухоли (превышающий его морфологический объем при МРТ), и идентифицируются субрегионы с более высоким риском рецидива, что влияет на запланированный объем стереотаксической терапии с расширенной зоной радиационного воздействия.
А возможность градации неоплазм по активности накопления радиоактивного маркера при ПЭТ перспективное направление для оптимизации расчета мощности облучения.
Направленная радиолигандная терапия новое перспективное применение метиона-11С и других аминокислотных радиотрассеров.
Наблюдение: преимущества метаболической оценки терапевтического ответа
Современным стандартом оценки нейроонкологической эффективности лечения является динамика МРТ с контрастным усилением. По определенным критериям ( Macdonald criteria, RANO criteria) определяется конкретный посттерапевтический эффект:
- Полный ответ;
- Истинная прогрессия;
- Псевдопрогрессия;
- Радиационное поражение;
- Псевдоответ
Согласно этим критериям, увеличение контрастного усиления ≥25% при МРТ является надежным признаком прогрессирования рака.
Тем не менее, контрастное усиление не может считаться специфичным после введения гадолиния, поскольку в первую очередь отражает пассаж контраста через поврежденный гематоэнцефалический барьер (ГЭБ).
Более того, у 20-30% пациентов проявляется так называемый эффект псевдопрогрессии, проявляющийся в патологическом усилении контрастирования при МРТ в первые три месяца после одновременного химио/радиационного лечения. Это связано с временным повышением проницаемости сосудистой сети опухоли после облучения, некрозами и инфарктами мозга после оперативного лечения и может усиливаться при проведении химиотерапии с темозоломидом (TMZ).
Связанный с лечением эффект затрудняет оценку результатов, вызывает сомнения в эффективности адъювантной терапии и может привести к ее преждевременному прекращению.
Пример:
ПЭТ и МРТ выполнялись 47-летнему пациенту до гистологического подтверждения диагноза глиобластомы (слева), через 8 недель (в середине) и через 3 месяца после завершения радиохимиотерапии темозоломидом (справа). МРТ через 8 недель после радиохимиотерапии показывают увеличение размеров опухоли. В отличие от этого, ПЭТ с 18F-FET демонстрирует пониженную метаболическую активность опухоли по сравнению с исходным ПЭТ, что указывает на псевдопрогрессию. Соответственно, контрольная МРТ, через 3 месяца после радиохимиотерапии показывает улучшение с регрессивными результатами без изменения схемы лечения (правая колонка).
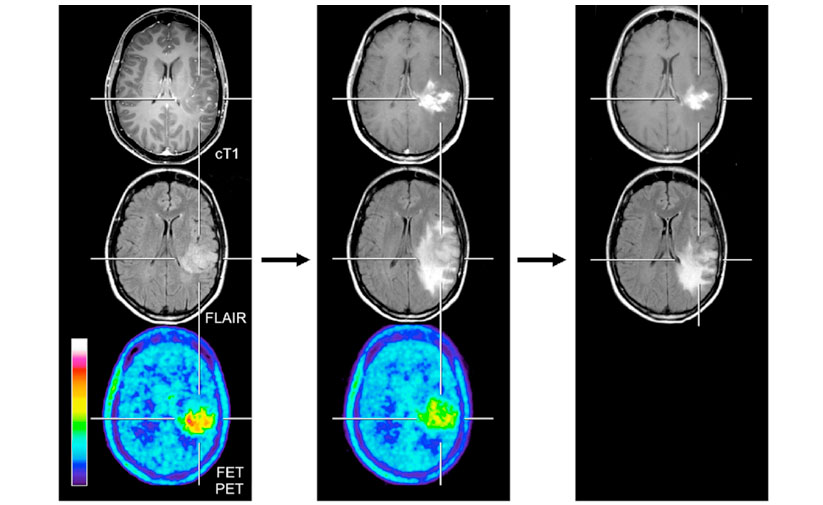
ПЭТ с тирозином позволило выявить псевдопрогрессию на МРТ
Еще один феномен потенциально нивелирует роль МРТ как основного метода контроля эффективности противораковой терапии. После введения антиангинальных препаратов (напр. бевацизумаба) в схему лечения, онкологи столкнулись с новым феноменом – псевдоответом. Эти средства вызывают заметное снижение контрастности уже через 1-2 дня после начала терапии, что, отчасти является результатом нормализации аномально проницаемых опухолевых сосудов, а не истинным противораковым эффектом. Нормализация проницаемости ГЭБ часто сочетается с уменьшением перифокального отека, улучшением неврологического статуса, что может приводить к преждевременной отмене противоотечной терапии при продолжающемся росте опухоли.
ПЭТ КТ с аминокислотными радиомаркерами способно предсказать ответ уже на начальном этапе лечения, что является предпосылкой персонализированного лечения адаптировать терапию для предотвращения неэффективного лечения.
Оборудование
Для исследования головного мозга используется аппаратура ведущих мировых производителей: GE Healthcare, Philips Healthcare, Siemens Healthcare, Toshiba Medical Systems. Это мощные гибридные системы позитронно-эмиссионной и спиральной компьютерной томографии позволяют провести высококачественное совмещение метаболических и анатомических изображений, что делает ПЭТ КТ золотым стандартом диагностики интракраниальных злокачественных образований.
На ПЭТ КТ сканах совмещаются метаболические и анатомические изображения